結合性軌道と反結合性軌道、HOMOとLUMO
結合性軌道と反結合性軌道
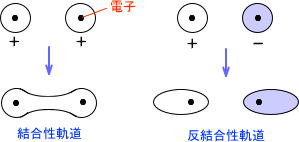
水素原子は原子単一としては存在せず、実際にはより安定なH2分子として存在する。このとき、水素原子は互いに1s軌道同士を重ねることで結合を形成している。
水素分子は電子を一つずつ出し合うことで結合を形成しているのであるが、一つ重要な事として「結合を形成するときは結合性軌道と反結合性軌道の二つの軌道ができる」ということを覚えておいてほしい。
では「結合性軌道・反結合性軌道とは何か」であるが、その名の通り結合性軌道は分子同士を結合させるようにする軌道であり、反結合性軌道とは分子同士の結合を開裂させるように働く軌道である。
「電子軌道」で記述したが、電子の存在確率は波動関数で表わされる。そして、同じ位相 (「 と 」「-と-」など同じ波) であるなら結合性軌道となり、逆位相の組み合わせ
( と-の波) であるなら反結合性軌道となる。
基本的に多くの物質はエネルギーの小さい方へと流れていく。好き勝手にエネルギーの高い不安定な状態をとろうとはしない。そのため、水素分子は二つの電子を結合性軌道に置き、安定な状態となっている。
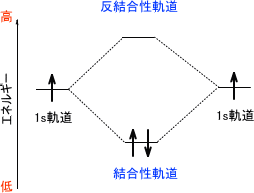
水素原子は電子を一つもっている。一つの軌道には電子が二つ入るため、二つの水素原子が電子を一つずつ出し合い、ちょうど結合性軌道に電子が二つ収まる形となる。
ここで電子を反結合性軌道に押し上げてしまうくらいのエネルギーを分子に与えた場合 (励起させた場合)、結合が開裂してしまうことがある。これは、反結合性軌道が結合性軌道による結合性を相殺してしまうためである。こう考えると、ヘリウムがなぜ単分子で安定であるのかを理解することができる。
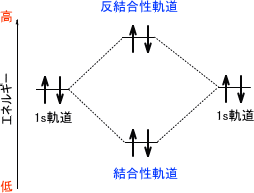
前述の通り、一つの軌道を形成しようとすると二つの軌道ができる。そして、一つの軌道には電子を二つしか収容することができない。ヘリウム原子は電子を二つもっているため、He2分子を形成しようとすると電子が反結合性軌道にまで入ってしまう。
反結合性軌道に電子が収容されるため、結合が開裂してしまうのである。これが、ヘリウムが分子で存在しない理由である。
HOMOとLUMO
ここでは、節という単語を覚えてほしい。反結合性軌道において電子が全く存在しない部分があり、ここを節という。
節 : 電子の存在確率がゼロとなる部分
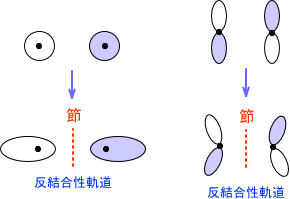
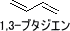
そして、「節には対称性がある」と理解しておけばよい。つまり、逆位相が合わさった場合に節ができる。実際に節を数えた方が分かりやすいと思うので、今回は1,3-ブタジエンのπ結合における節を数えてみたいと思う。
まず、1,3-ブタジエンにはπ電子が四つある。そして、それぞれπ電子同士がπ結合を形成することによって二重結合が生じる。
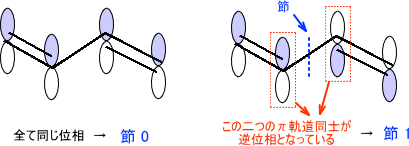
全て同じ位相であれば節の数はゼロである。しかし、逆位相があると節が生じてしまう。節では電子の存在確率がゼロとなっており、よりエネルギーが高く不安定な状態となる。なお、上の右図では、節を軸にして二つのπ軌道同士が対称に描かれていることが分かる。これが、「節には対称性があると理解しておけばよい」と述べた理由である。
1,3-ブタジエンではπ電子によってπ結合が二つ形成されている。一つの結合が形成されるとそれぞれ結合性軌道と反結合性軌道が生じる。「π結合が二つ形成されている」ということは結合性軌道と反結合性軌道がそれぞれ二つずつ生じていることが分かる。つまり、下の図のような四つの軌道を考える事が出来る。
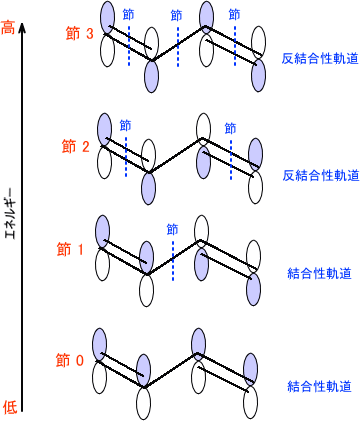
一つの軌道には二つの電子を収容することができる。1,3-ブタジエンはπ電子を四つもっているため、二つの結合性軌道に電子を二つずつ収容することができる。このとき結合性軌道は電子で満たされ、反結合性軌道は電子が空の状態となっている。
ここで、HOMOとLUMOの説明をしたいと思う。HOMOは「Highest Occupied Molecular Orbital」のことであり、日本語では最高被占軌道と言われている。つまり電子が存在している軌道のうち、最もエネルギーが高い軌道のことを指す。1,3-ブタジエンの軌道を示している下の図で青色で囲んでいる軌道がHOMOとなっている。
それに対し、LUMOは「Lowest Unoccupied Molecular Orbital」のことであり、最低空軌道と訳される。LUMOは電子がない空の軌道のうち、最もエネルギーの低い軌道のことを指す。
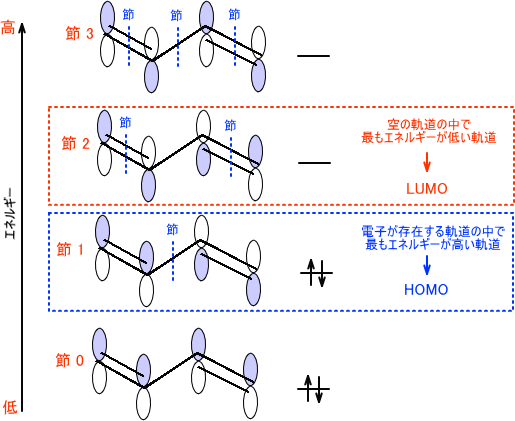
これらが結合性軌道・反結合性軌道、HOMO・LUMOそして節の簡単な考え方である。
スポンサードリンク
カテゴリー
スポンサードリンク
