生体エネルギー、生体酸化
生態エネルギー
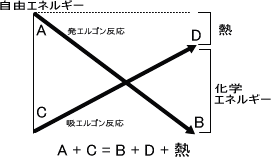
・発エルゴン反応と吸エルゴン反応
自由エネルギー変化において⊿G<0であるならば、その反応は自然に進む。これは発エルゴン反応である。
自由エネルギー変化において⊿G>0であるならば、その反応は自然に進まない。これは吸エルゴン反応である。
発エルゴン的な反応は異化で、吸エルゴン的な反応は同化である。
自然に進まない反応(吸エルゴン反応)を進めるために、自然に進む反応(発エルゴン反応)が反応するときに発生するエネルギーを吸エルゴン反応に使用することで吸エルゴン反応を反応させ、生体反応を進める。これを共役という。
ATP(Adenosine Tri Phosphate)
ATP → ADP Pi 、 ADP → AMP Pi Pi はリン酸
ATP加水分解エネルギーは他と比べると中程度である。この理由は高エネルギーすぎると、無駄になるエネルギーが多くなるからである。
例えば、500円のものを買うとする。生体反応ではおつりがでないので、1000円だすのと10000円だすのではエネルギーの無駄の差は明らかである。これは、エネルギー交換において重要な意味をもつ。
ATPの合成には解糖、酸化的リン酸化などがある。
高エネルギーリン酸結合
ATPはリン酸が3個、ADPはリン酸が2個つながっている。高エネルギーリン酸結合とはリン酸とリン酸の結合でありATPは2個、ADPは1個の高エネルギーリン酸結合をもつ。リン酸結合が切れることにより生じるエネルギーを生体反応に利用する。
生体酸化
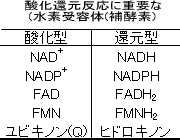
酸化還元反応に関与する酵素を酸化還元酵素という。酸化還元酵素は次の4種類に分類される。
・酸化酵素(オキシダーゼ:oxidase)
・脱水素酵素(デヒドロゲナーゼ:dehydrogenase)
・ヒドロペルオキシダーゼ((hydroperoxidase)
・オキシゲナーゼ(oxigenase)
ミトコンドリア
外膜と内膜からなり内膜はクリステ、内膜に囲まれた空間はマトリックスと呼ばれる。
クリステ
ひだ状構造物でATP合成酵素のATP/ADP交換輸送体や呼吸鎖(電子伝達系)がある。
マトリックス
クエン酸回路等の代謝酵素がある。
呼吸鎖(電子伝達系)
低い酸化還元電位を持つNADH等から高い電位をもつO2へと電子を伝達する。
NADH → 複合体Ⅰ(NADHデヒドロゲナーゼ) → ユビキノン(Q) →
複合体Ⅲ(シトクロムbc1) → シトクロムc(Cyt c) → シトクロムオキシダーゼ → O2
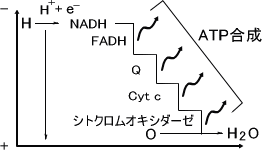
水素の酸化は段階的に起こる。この理由も前述の例で説明したお金の話と同じ理由です。これは、大きなエネルギーを効率よく転換(共役)させるのに重要である。
化学浸透圧説
シャトルによりミトコンドリアの内膜(クリステ)に入ったNADHは呼吸鎖に入る。呼吸鎖では酸化還元電位の低いものから高いものへと水素(電子)が伝達する。このとき、1つのNADHで3つのH+を外へだす。
内膜はふつうイオンを通さないので、膜の外と内でプロトン(H+)による濃度勾配が生じる。これにより、水素イオン濃度差による電気化学的ポテンシャルが生じる。
そして、F0-F1サブユニットをH+が通過した後にATPシンターゼによりATPが合成される。合成されるときのエネルギーとして、このポテンシャルが利用される。
この一連のATP合成の方法を化学浸透圧説という。

脱共役剤(アンカップラー)
ATP合成にはミトコンドリア内膜の内外のプロトン濃度勾配により生じる電気化学的ポテンシャルが必要である。しかし、脱共役剤はプロトンを勝手に内膜の内側に入れるため濃度勾配が少なくなり、反応が進みにくくなる。
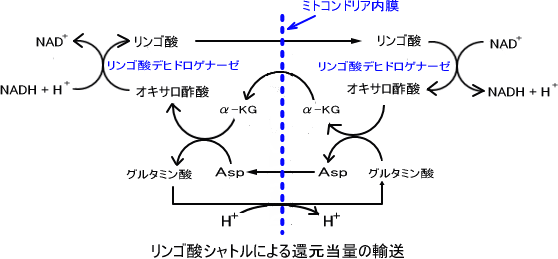
リンゴ酸シャトル
NADHはミトコンドリア内膜を通過できない。NADHの還元力をどうにかしてミトコンドリア内に入れる役割をしているのがリンゴ酸シャトルである。
ただし、外にあるNADHが直接ミトコンドリア内に入るのではない。外にあるNADHを使って特定の物質を介し、ミトコンドリア内にあるNAD+をNADHに変換することによって、還元力を移行させるのである。
まず外にあるNADHを使ってオキサロ酢酸を還元し、内膜を通過できるリンゴ酸に変える。内膜を通過したリンゴ酸はミトコンドリア内に入り、リンゴ酸デヒドロゲナーゼにより酸化されオキサロ酢酸になる。これにより内側のNAD+をNADHに還元するのである。
またオキサロ酢酸は内膜を通過できないので、α-KG(α-ケトグルタル酸)に変えられ膜を通り再びオキサロ酢酸となる。
スポンサードリンク
カテゴリー
スポンサードリンク
