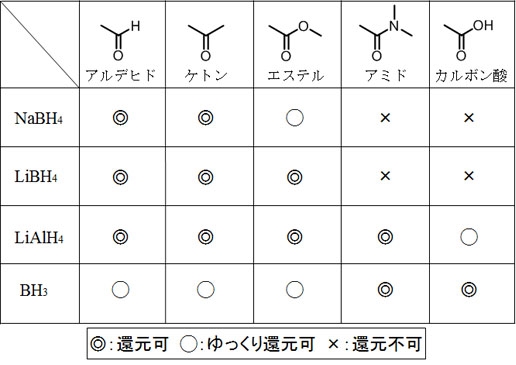
ヒドリド還元剤によるカルボニル基の還元
カルボニル基の還元を行うとき、カルボニル基の構造や用いる還元剤によって反応速度が異なったり、反応しなかったりする。そのため、構造式に同じようにカルボニル基が存在していたとしても、使用する還元剤によって目的とするカルボニル基だけを選択的に還元することが可能となる。
必要とする化合物を合成するためには、その目的に合わせて使用する還元剤を選ぶ必要がある。
反応機構
・アルデヒド、ケトンからのアルコールへの還元
代表的な試薬は、水素化ホウ素ナトリウム(NaBH4)と水素化アルミニウムリチウム(LiAlH4)である。どちらも、アルデヒド、ケトンをアルコールへと還元するが、LiAlH4は反応性が高く、水と触れると発火することから、主にNaBH4が用いられる。
これらは、どちらもヒドリド還元剤とも呼ばれ、ヒドリド(H-)の移動を伴う反応である。
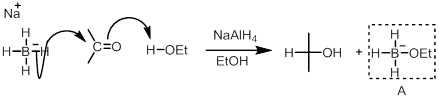
反応過程で生じる水素化アルコキシホウ素アニオン(図中A)は、還元剤として働くため、理論的には、1分子のNaBH4からカルボニル体4分子が還元される。
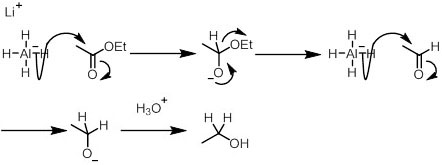
・エステルからアルコールへの還元
代表的な試薬は、LiAlH4である。カルボン酸やアミドが存在している場合には、水素化ホウ素リチウム(LiBH4)あるいは、NaBH4が用いることでエステルだけを選択的にアルコールへと還元できる。
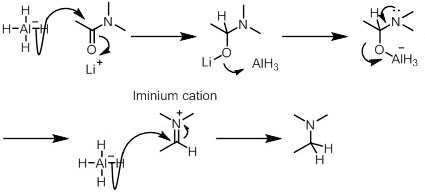
・アミドからアミンへの還元
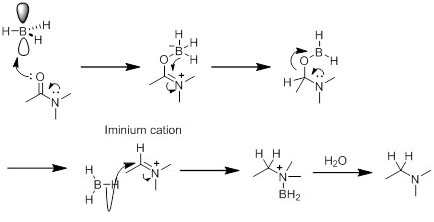
LiAlH4が用いられる。エステルの還元と似ているが、エステルの還元とは異なり、途中イミニウムイオンを介して反応が生じる。
また、ボラン(BH3)も、しばしばアミドの還元に用いられる。BH3は、空のp軌道を有しており、そこに電子対を受け入れルイス酸として働く。つまり、電離不足なエステルのカルボニル基よりも電子豊富なカルボン酸やアミドのカルボニル基と速やかに反応する。
・カルボン酸からアルコールへの還元
BH3とLiAlH4が代表的な還元剤である。
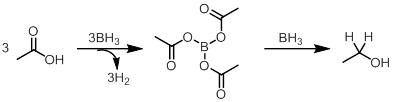
カルボン酸とBH3は、水素を発生させながら反応し、中間体のアシルボロートとなる。この中間体の反応性は高く、BH3と反応することで、アルコールを生じる。
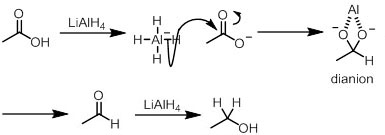
一方で、LiAlH4によるカルボン酸の還元は、高温で長時間を有する。LiAlH4は、塩基としても働くため、ヒドリドはカルボキシラートイオンに対して攻撃し、中間体のジアニオンを生じる。この中間体では、二つの酸素がAlに配位しており反応は起こりづらい。
したがって、アルデヒドへの反応に高温長時間を有する。
・エステルとアミドからアルデヒドへの還元
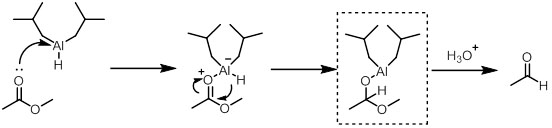
エステルから直接、一反応でアルデヒドへ還元するときの代表的な試薬として、水素化ジイソブチルアルミニウム(DIBAL)がある。DIBALは二量体として存在する。
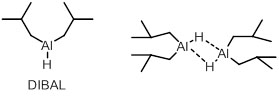
DIBALはアルミニウム上に空p軌道を有しており、ルイス酸性を有し、ボランの反応機構とよく似ている。DIBALでの還元は低温で行われ、低温で安定な中間体を処理することでアルデヒドが生成する。
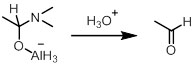
アミドからアルデヒドへの還元ではLiAlH4が用いられる。先に示したアミドからアミンへの還元の中の中間体は、低温で安定である。これを水で処理することで、アルデヒドが生じる。
スポンサードリンク
カテゴリー
スポンサードリンク
