有機化学の反応性:アルキルへの反応
共役ジエンへの付加反応
共役ジエンは共役していないジエンよりも安定なだけではない。共役ジエンの付加反応は特殊な反応を示す。例えばbuta-1.3-dieneに臭化水素を付加させると3-ブロモブタ-1-エンと1-ブロモブタ-2-エンの二つの化合物を得ることができる。
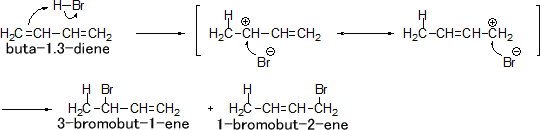
反応するときの温度が低温(-80℃)であるなら生成物は1,2-付加が主であり、1,2-付加物が約80%、1,4-付加物が約20%の割合で生成する。
反応温度を高く(40℃)にすると今度は主な生成物が1,4-付加になる。このとき1,2-付加物が約20%、1,4-付加物が約80%の割合で生成する。
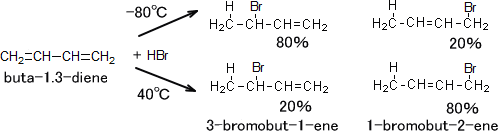
温度によって生じる反応性生物の割合の違いは、反応速度と最終生成物の安定性によるものである。つまり、1,4-付加反応よりも1,2-付加反応の方が反応速度が速い。しかし最終生成物は1,4-付加物の方が安定である。下にエネルギー図を示す。
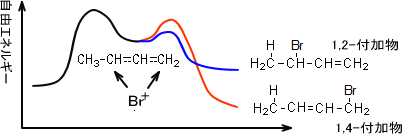
図を見れば分かるとおり第二段階の反応において、1,2-付加反応の方が反応に必要なエネルギーが少ない。低温では1,4-付加反応が起こるために必要なだけのエネルギーをもっていないため、エネルギー障壁の小さい(反応速度の速い)1,2-付加反応が優先的に起こる。
温度を高くすれば1,4-付加反応するために必要なエネルギーをもつようになる。すると、1,2-付加物よりも安定な1,4-付加物の生成が多くなる。
重要なのはこの反応が可逆的であることである。
温度を低温にして1,2-付加物を生成させた後、温度を高くすると1,4-付加物の割合が多くなる。1,2-付加反応ではエネルギー障壁を越えて反応する速度が速いが、第二段階の反応で臭素イオンが結合する前のアリルカチオンに戻る反応も速い。
生成物はより安定になろうとする。そのため、温度が高いと1,2-付加物からアリルカチオンに戻ったあとに1,4-付加物に変わる。
付加環化反応
共役ジエンにアルケンを反応させると1,4-付加反応する。これにより、環状化合物が生成する。
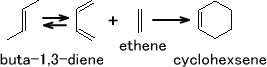
アルケンの酸化開裂反応
オゾンや過マンガン酸カリウムなどの酸化剤をアルケンと反応させると開裂反応が起こる。これによって、アルコール、アルデヒド、ケトン、カルボン酸が生成する。
・オゾンによる酸化開裂
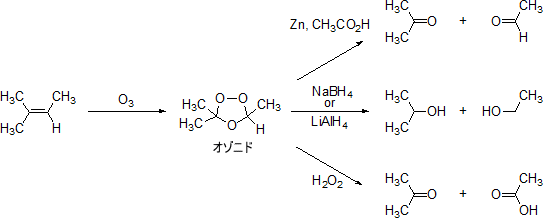
まず、アルケンにオゾン(O3)を作用させると複数の過程を得てオゾニドとなる。このオゾニドを亜鉛と酢酸で処理するとアルデヒドかケトンを得ることができる。
また、テトラヒドロホウ素ナトリウム(NaBH4)またはテトラヒドリドアルミン酸リチウム(LiAlH4)で処理した場合は2種類のアルコールを得ることができ、過酸化水素で処理するならカルボン酸かケトンを得ることができる。
・過マンガン酸カリウムによる酸化開裂
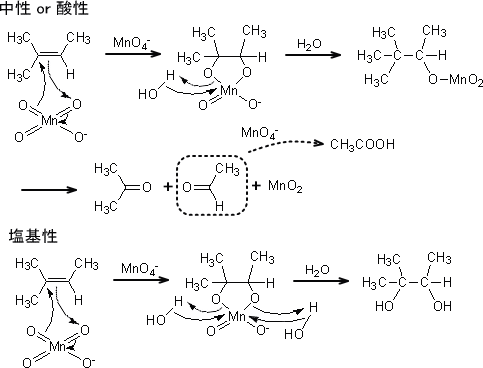
アルケンを中性または酸性の条件下で過マンガン酸カリウムと反応させると、二重結合が切断されてケトンまたはカルボン酸を得る。しかし、塩基性の条件下であるとcis-1,2-ジオールを得る。
アルキンの反応
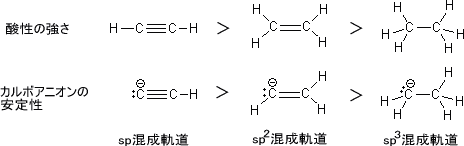
エチン、エテン、エタンはそれぞれ三重結合、二重結合、単結合をもつ。この3つの物質の酸性の強さを比較するとエチン>エテン>エタンとなる。これは塩基によって「プロトンが引き抜かれた」と仮定したときの安定性の違いによるものである。
エチン、エテン、エタンのプロトンがそれぞれ引き抜かれたとき、生成するカルボアニオンはエチン>エテン>エタンの順で安定である。プロトンがなくても安定なので、プロトンが遊離しやすくなり酸性の強さが増すのである。
これはs性の違いによって起こる。プロトンが引き抜かれた孤立電子対がエチンの場合はsp混成軌道に、エテンはsp2混成軌道に、エタンはsp3混成軌道に入っている。sp混成軌道のs性は50%、sp2混成軌道のs性は33.3%、sp3混成軌道のs性は25%である。
一般にs軌道の方がp軌道よりも電子をより核に引き付ける。そのためエネルギーが低くなり、安定となる。これが酸性の強さが違う理由である。
・末端アルキンのアルキル化反応
前述の通り、末端アルキンの水素はアルカンやアルケンの水素よりも遊離しやすい。つまり、強塩基で処理するとカルボアニオンになりやすい。ここで第一級ハロアルカンと反応させると置換アルキンとなる。
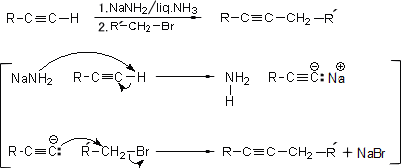
アルキンへの付加反応
・リンドラー触媒
アルキンからアルケンを生成するとき、触媒の作用を抑える必要がある。触媒の作用が強いとアルキンから一気にアルカンが生成するからである。
リンドラー触媒はアルキンからアルケンを生成することが可能な触媒であり、シン付加が優先的に進む。
・バーチ還元
リンドラー触媒からはcis-アルケンを生成することができるが、trans-アルケンを生成したい場合はバーチ還元を用いる。
これは液体中にアンモニアが存在する状態で、アルキンをナトリウムまたはリチウムと反応させることによって起こる。なお、この反応は低温で行う必要がある。
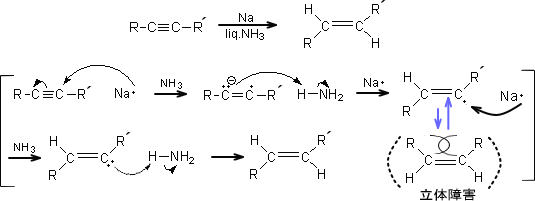
アルキンの水素化反応は次のようになる。
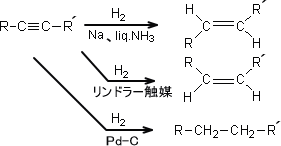
なお、アルキンにハロゲン化水素が付加する場合、反応は位置選択性でありマルコウニコフ則に従う。しかしヒドロホウ素化反応をすると反マルコウニコフ則となり、アルデヒドを得ることができる。
スポンサードリンク
カテゴリー
スポンサードリンク
