核磁気共鳴(NMR)の基礎
現在、NMR法は有機化合物の構造決定において広く利用されている方法である。NMR法では構成原子の水素と炭素の構造上の情報を与えてくれる。
NMRは吸収スペクトルである。NMRにはラジオ波が使用されており、原子核のスピン状態を測定している。測定の対象としては1Hと13Cがある。ただし、質量数2の水素(2H)などのほかの原子の測定も可能である。
NMRは水素や炭素上の微妙な違いを測定する。横軸の単位には(ppm)を用いる。
ゼーマン分裂
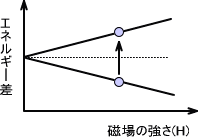
ただ単に原子核にラジオ波を照射しても変化はない。変化を見るには磁場におく必要があり、核に磁場が与えられると二つのエネルギー順位に分裂する。これをゼーマン分裂という。
この説明だけでは「ゼーマン分裂」の意味がさっぱり分からないと思うので、以下にゼーマン分裂をきちんと説明しようと思う。
まず、一つの軌道に存在する電子は二つの自転状態を取ることが可能である。磁場がない状態ではこの二つの状態は同じエネルギーである。しかし、ここに磁場をかけると二つの状態にエネルギーの差ができるのである。
それでは、なぜ磁場をかけることでこのようなエネルギーの差がでるのだろうか。
電子は電荷をもっており、この電子は回転している。電荷をもつ物質が回転すると磁力が生じるはずである。つまり、電子は小さな磁石(S極、N極が存在)なのである。ここに磁場がかかれば、小さな磁石である電子はエネルギーに差が出てしまう。
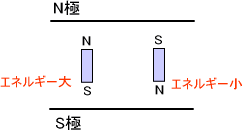
このようにゼーマン分裂やスピンを扱う場合には「場」が重要になってくる。
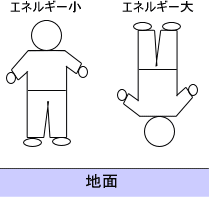
例えば、ヒトが普通に立っている場合と逆立ちしている場合では、逆立ちしている場合の方がエネルギーが高いはずである。
しかし、宇宙空間では上下という概念が存在しない。つまり、上下でエネルギーに差がない。これは、宇宙には「重力」という場が存在しないためであり、これが地球であると上下でエネルギーに差が出てしまう。
これは電子にも同じことが言える。磁場が存在しなければ、二つの状態にエネルギー差はない。しかし、磁場が存在すれば状態が異なる二つにはエネルギーに差がでてしまう。
また、地球と月では月の方が上下のエネルギーの差が小さいはずである。これは月の方が重力が小さいためである。同じように、磁場の強さが強いほど分裂の度合いも大きくなる。
核スピンは通常、低いエネルギー状態をとっている。しかし、エネルギー差と等しいラジオ波が照射されると、吸収してエネルギーが高い状態に移動する。
NMRの原理 (1H-NMR)
ここでは1H-NMRについて説明する。まず、NMRとはプロトンの周りの電子密度を測定する機械である。
何もしていない状態の分子は個々の原子でさまざまなエネルギー状態をとっている。ベクトルで表すと、下(左図)のようにいろいろな方向を向いているのである。
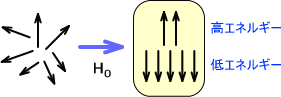
そして、この状態の分子を大きな磁石の中に入れると、上(右図)のように二つの状態のエネルギーに分かれる。このとき、低エネルギーと高エネルギーの状態が存在する。当然、低エネルギー状態をとる場合の方が多い。
ここで外部エネルギーを与えると、下の図のように全て高エネルギー状態にさせる点が存在するはずである。
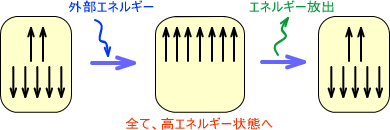
なお、ピークが表れるのは外部エネルギーを与えて、「全て高エネルギー状態」になったときである。高エネルギー状態となった後は、エネルギーを放出してもとの状態に戻る。
このとき、NMRは外部エネルギー量かエネルギー放出量のどちらかを測定する。つまり、NMRには「与えた外部エネルギー量で判断するもの」と「放出されたエネルギー量を判断するもの」の二種類がある。
・電子密度によるスペクトルの違い
そもそも、測定したいプロトンはどれも同じ1Hであるため、どれも性質は同じである。しかし電子密度は異なっており、NMRはこの電子密度の差を見極める。
例えば、プロトンに「10」の外部エネルギーを与えると高エネルギー状態となり、スペクトルが観測されるとする。このとき、プロトンの周りには電子が存在しており、この電子が外部磁場を遮断してしまう。すなわち、「電子がバリアーとして働く」と考えればよい。
つまり「10」の外部エネルギーを与えても、このバリアーがあるためスペクトルは観測されないのである。もし、電子のバリアーが「2」のエネルギー分だけ防御するのであれば、「12」の外部エネルギーを与えるとスペクトルが観測される。
そして、このバリアーの強さは電子密度によって異なる。当然、電子密度が大きければ、電子によるバリアーの影響は大きくなる。
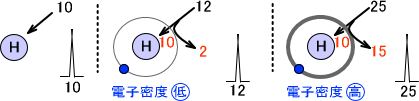
電子密度が小さいほど低磁場でスペクトルが観測され、電子密度が高いほど高磁場でスペクトルが観測される。
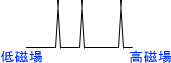
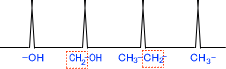
例として、「CH3CH2CH2OH(プロパノール)」を下の図のようにそれぞれの炭素原子,酸素原子に番号をつけて説明したいと思う。
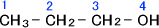
このとき、2番のプロトンと3番のプロトンではどちらが低磁場に表れるであろうか。
2番の炭素原子の隣にはメチルがあり、電子を押し出されている状態である。そのため、電子密度が高い。それに対し、3番の炭素原子の隣にはO(酸素原子)があるため、電子を引っ張られている状態である。つまり、電子密度が低い。
このように考えると、電子のバリアーが弱い(電子密度の低い)3番の炭素原子のプロトンの方が低磁場側に表れることが分かる。
このように電子密度を考えると、どのプロトンが低磁場側(or高磁場側)に表れるかを予測することができる。例えば、プロパノールの場合では下のようになると予想できる。
・磁気遮へいと化学シフト
水素がラジオ波を吸収するとしても、すべての水素が同じような吸収をしたのでは構造解析はできない。しかし、実際には水素によってラジオ波の吸収が異なっている。これはそれぞれの核を取り巻く電子の環境が異なるからである。
核の周辺に外部磁場がかかったとき、回転している電子はそれ自身の微少磁場を利用して外部磁場を弱めるように働く。そのため核に影響する磁場は弱くなり、共鳴周波数は小さくなる。この現象を磁気遮へい効果という。
磁気遮へいの程度は水素の置かれた環境によって異なる。そこで、基準物質からどれくらい差があるかを表すのが化学シフトである。この基準物質には有機化合物の中で磁気遮へい効果が最も大きいテトラメチルシラン(TMS)が用いられる。
・カップリング(非等価な場合)
カップリングとは隣の炭素にある水素の情報を表したものである。ある炭素にプロトンが結合している場合、そのプロトンのスペクトルは一本のシグナルとして観測される。しかし、隣の炭素にプロトンが結合していると、そのプロトンの影響を受けてしまうのである。
もし隣の炭素にHが一つあるなら、共鳴線は二重線として表れる。
例えば、それぞれ下のようなA,Bの構造の分子があるとする。
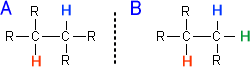
Aの分子でHに注目した場合、隣の炭素にプロトン(H)が一つ結合していることが分かる。プロトンは一つのピークを二つのピークに分ける性質がある。そのため、二重線として観測される。
また、Bの分子のHに注目した場合、隣の炭素に結合しているプロトンはHとHの二つである。一つ目のプロトンは一本の線を二重線にする。また二つ目のプロトンは、二重線をさらに二つずつに分けるので四重線にする。つまり、四重線のピークで表れるのである。

隣の炭素にあるプロトンの数をnとすると、2nの本数に分裂してスペクトルが観測される。これがカップリングの基本である。
・プロトンが等価な場合のカップリング
先ほど説明したカップリングには例外がある。前述のカップリングは、「HとHが等価でない(性質が同じでない)」という条件がある。そして、もしHとHが等価であるなら分裂する本数は異なってくる。
「プロトンが等価な場合のカップリング」を説明する前に、覚えてもらいたいものがある。それは、J値(カップリングコンシスタント:結合乗数)である。
J値は分裂したシグナル間の距離であり、Hz(ヘルツ)で表す。

「等価な場合のカップリング」を、前述の「カップリング(非等価な場合)」で説明したA,Bの分子で説明しようと思う。なお、プロトンは全て等価である。
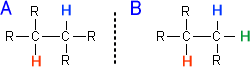
Aの分子でHに注目した場合、スペクトルは二重線で表れる。このときのJ値を12Hzとする。
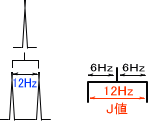
Bの分子でHに注目した場合、隣の炭素に二つの等価なプロトン(HとH)が結合していることが分かる。二つとも同じ性質であるため、二重線は同じJ値(ここでは12Hz)で二つずつに分かれるはずである。
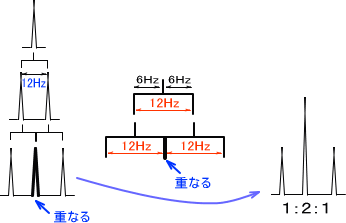
同じJ値で分かれるため、真ん中で二つのシグナルが重なってしまう。このため、スペクトルは4本ではなく、3本で出る。また、重なっているので1:2:1の面積比となる。
このようにプロトンが等価な場合、隣の炭素にあるプロトンの数をnとすると、n 1の本数に分裂してスペクトルが観測される。
・積分比
積分比とは、つまり面積比のことである。(ここでの積分比の説明は、プロトンが等価な場合を考える)
隣の炭素にHが一つあるなら、そのHのスピンの状態には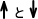 の二種類がある。つまり、二重線で表れる。
の二種類がある。つまり、二重線で表れる。
隣の炭素にHが二つある場合、スピンの状態は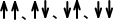 の四種類がある。ただし、
の四種類がある。ただし、 はエネルギー的に同じであるため面積比が1:2:1の三重線として表れる。同じように隣の炭素にHが三つある場合を考えると、下のように面積比が1:3:3:1の四重線として表れる。
はエネルギー的に同じであるため面積比が1:2:1の三重線として表れる。同じように隣の炭素にHが三つある場合を考えると、下のように面積比が1:3:3:1の四重線として表れる。
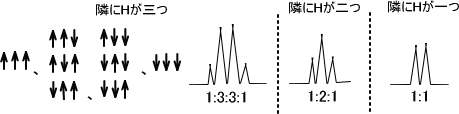
積分比で何が分かるかというと、プロトン比が求まるのである。なお、プロトンの数ではなくてプロトンの比であることに注意しないといけない。
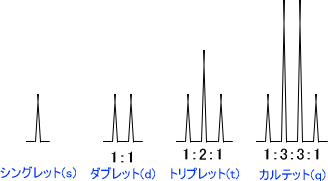
また、それぞれ一本のピークをシングレット(s)、二重線をダブレット(d)、三重線をトリプレット(t)、四重線をカルテット(q)という。ただし、1:2:1の面積比をもつ場合のみをトリプレットといい、1:3:3:1の面積比をもつ場合のみをカルテットという。
デカップリング
デカップリングとは、カップリングをなくしてしまうことである。カップリングしなくなるので、ピークは必ずシングレットで表れる。
NMRの装置には、「与えた外部エネルギー量で判断するもの」と「エネルギー放出量を判断するもの」の二種類があると述べた。ここでは、分かりやすいように後者のNMR装置の場合で説明する。
外部エネルギーを与えると、ある特定の値でスペクトルを観測することができる。このときの電子は高エネルギー状態にある。高エネルギー状態から、通常の低エネルギー状態に移行するときにエネルギーを出す。
この放出されるエネルギーをNMRで測定するのだが、エネルギーを放出されないようにすればNMRで測定されないはずである。
ケミカルシフト(化学シフト)するエネルギーを与え続けていれば、高エネルギー状態が永遠と続いてしまう。つまり、エネルギーは放出されない。エネルギーが放出されないのでNMRで測定されないのである。
ところで、下のような構造式をもつ分子があるとする。
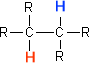
Hに注目すると、となりの炭素にあるプロトンはHだけであることが分かる。つまり、ダブレットのピークが観測される。デカップリングでは、通常ではダブレットでピークが出るのを、無理やりシングレットのピークにしてしまうのである。(トリプレットやカルテットなどのピークもシングレットとなる)
隣の炭素にHがあるためダブレットになるのだから、Hの影響がでないようにしてやればシングレットとなる。
Hのピークをシングレットにするためには、Hがケミカルシフト(化学シフト)するエネルギーを照射し続けながら測定すればよい。これによってHの影響がなくなり、カップリングしなくなる。
なお、「与えた外部エネルギー量」で判断するNMRの場合でもデカップリングは可能である。
それでは、デカップリングをすることでどんな良いことがあるのだろうか。これには、「カップリングしているために複雑になっているピークを分かりやすくする」という効果がある。
例えば、「CH3-CH2-CH2-CH2-CH2-OH(ペンタノール)」があるとする。
赤色をつけたプロトンは性質が似ており、ピークを見てもどちらかが分かりにくい。なお、プロトンは等価であり、両方とも隣の炭素にあるプロトン数は4であるため、ピークは5本に分かれて出る。
このとき、「CH3-CH2-CH2-CH2-CH2-OH」の緑で示したプロトンをデカップリングによってカップリングさせないようにすると、青色で示したプロトンのピークは隣の炭素にあるプロトン数が見かけ上2となるため、3本のピークで表れる。
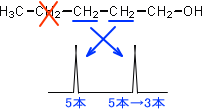
このように、デカップリングによってどのプロトンによるピークかを簡単に見分けることができる。
13C-NMR
12CはNMRで測定できないが、13CはNMRによって測定可能である。
プロトンは13Cの影響を考えなくてもよいが、13Cはプロトンの影響を考えないといけない。また、13Cの存在比は約1%であり、自然界に少ない。そのため、感度が低いのである。
プロトンでの化学シフトは約10ppmの値までである。しかし、13Cの化学シフトの値は200ppmまでと、プロトンの化学シフトと比べてとても範囲が広い。このような理由があるため、たとえ同じ機械で測定したとしても1Hと13Cのスペクトルが重なることはない。
スポンサードリンク
カテゴリー
スポンサードリンク
